の 北米整形外科市場 そしてアジア太平洋地域は、世界の整形外科医療機器業界において戦略的に最も重要な2つの地域であるが、構造、価格設定、規制制度、成長可能性において大きく異なっている。.
グローバル展開を目指す製造業者、OEM/ODMパートナー、および販売業者にとって、 北米とアジアの整形外科市場の比較 これは、情報に基づいた投資、製品、および規制に関する意思決定を行う上で不可欠です。.
この記事は、世界の整形外科分野に関する包括的なガイドの一部です。以下では、両市場を詳細に分析し、主要な側面から体系的な比較を行います。.
🌎 北米整形外科市場:規模、成熟度、およびプレミアム市場の動向
💰 北米整形外科市場における市場規模と成熟度
の 北米整形外科市場, 米国が支配する整形外科市場は、依然として世界最大かつ最も成熟した市場である。2026年の総収益は、 230億~250億米ドル, 約 世界の整形外科用医療機器売上高の38~40%.
市場はいくつかの重要な特徴によって定義されます。
- 🏥 施術件数が多い
米国では年間約120万件の人工股関節置換術と約140万件の人工膝関節置換術が実施されており、これは確立された外科医療インフラを反映している。. - 💎 プレミアム製品への嗜好
外科医や病院は、長期的な臨床的証拠に裏付けられた実績のあるインプラントシステムを強く支持しており、ブランドの評判は成功の重要な要素となっている。. - 📦 委託販売型流通モデル
ほとんどのインプラント会社は病院施設内に在庫を直接保管しており、多額の運転資金を必要とする資本集約型の流通モデルとなっている。. - 💳 複雑な償還制度
医療機器の購入決定は、メディケアのDRG(診断群分類)に基づく償還率、民間保険会社との契約、および包括払い制度によって影響を受ける。.
これらの要因により 北米整形外科市場 非常に収益性が高いが、同時に競争も激しく、運営面でも非常に要求が高い。.
🧾 北米整形外科市場におけるFDA規制枠組み
アクセス 北米整形外科市場 米国食品医薬品局(FDA)の厳格な規制経路への準拠が求められます。
- ⚙️ クラスII機器(510(k))
ほとんどの外傷用インプラントや多くの関節システムはこのカテゴリーに分類され、既存の先行デバイスとの実質的な同等性を証明する必要がある。. - 🧪 クラスIII医療機器(PMA)
新規インプラントには、完全な臨床試験と市販前承認が必要です。このプロセスには通常、費用がかかります。 100万~500万米ドル以上そして、 3~7歳. - 🔍 デノボ経路
先行事例はないものの、低リスクから中リスクに分類される革新的な医療機器に適用される。.
👉 外部参照: FDA医療機器
🏭 北米整形外科市場におけるOEM事業機会
大手多国籍ブランドが市場を席巻しているにもかかわらず、OEMおよびプライベートブランドの機会は依然として有望である。
- 🔧 手術器具および付属システム
- 📦 滅菌トレイ、包装、物流関連部品
- 💡 外来手術センター(ASC)を対象とした、低価格帯のインプラントシステム
- 📉 グループ購買組織(GPO)チャネルで競合する汎用外傷インプラント
これらのニッチ市場により、小規模またはコスト重視のメーカーが参入することが可能になります。 北米整形外科市場 プレミアム層で直接競合することなく。.
🌏 アジアの整形外科市場:構造的複雑性を伴う高成長
📈 アジア整形外科市場の成長動向と地域別推進要因
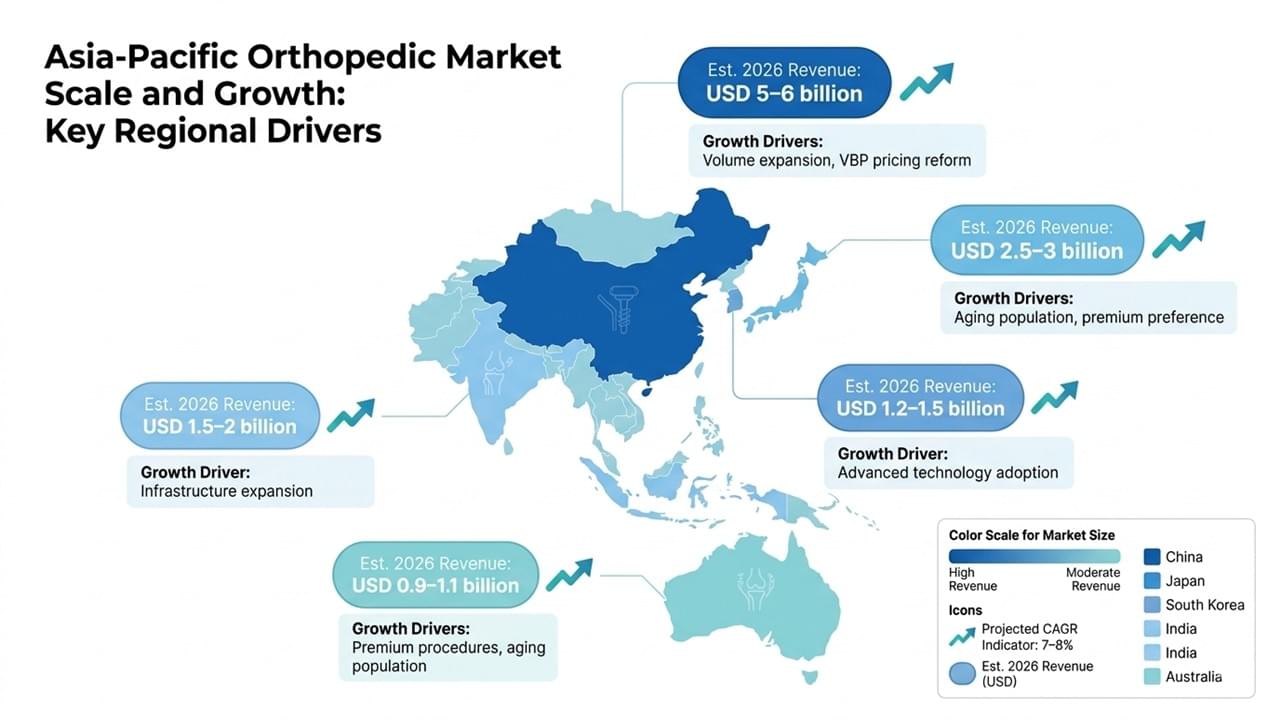
の アジアの整形外科市場 約 2026年には130億~140億米ドル。, 予測される 2030年までの年平均成長率(CAGR)は7~8%, 北米を大きく上回るペースで増加している。.
地域需要の大半を占めるのは以下の5カ国である。
| 国 | 2026年までの収益 | 主要な成長要因 |
| 中国 | 50億~60億米ドル | ボリューム拡大、VBP改革 |
| 日本 | 25億~30億米ドル | 高齢化社会 |
| 韓国 | 12億~15億米ドル | 先進技術の導入 |
| インド | 15億~20億米ドル | 医療インフラの拡張 |
| オーストラリア | 9億~11億米ドル | プレミアム手順 |
これらの数字は強い アジアの整形外科市場の成長動向, 人口動態の変化、政策改革、医療へのアクセス拡大などが要因となっている。.
⚖️ 整形外科用医療機器の規制の違い:FDAとアジアの整形外科市場
特徴的なのは 北米とアジアの整形外科市場の比較 規制の多様性である。.
- 🇨🇳 中国(NMPA)
クラスIIIインプラントには、長期間にわたる登録手続きが必要です。 3~5歳. 数量ベース調達(VBP)プログラムにより、インプラント価格は最大で 80–90%, 国内市場シェアの拡大を加速させている。. - 🇯🇵 日本(医薬品医療機器総合機構)
多くの場合、現地の臨床データ(「ブリッジ試験」)が必要となり、承認までの期間は通常 FDAより12~18ヶ月長い. 市場は、実績のある高品質な製品を強く支持している。. - 🇮🇳 インド(CDSCO)
2017年医療機器規則に基づき、規制要件が強化されました。市場は依然として価格に敏感ですが、販売代理店主導の参入により急速な成長の可能性を秘めています。. - 🇰🇷 韓国(食品医薬品安全処)
ロボット工学やナビゲーションシステムなどの先端技術を迅速に導入することで知られています。ISO 13485に準拠した品質システムが求められます。.
👉 外部参照: WHO医療機器ガイダンス
⚔️ 北米とアジアの整形外科市場の比較
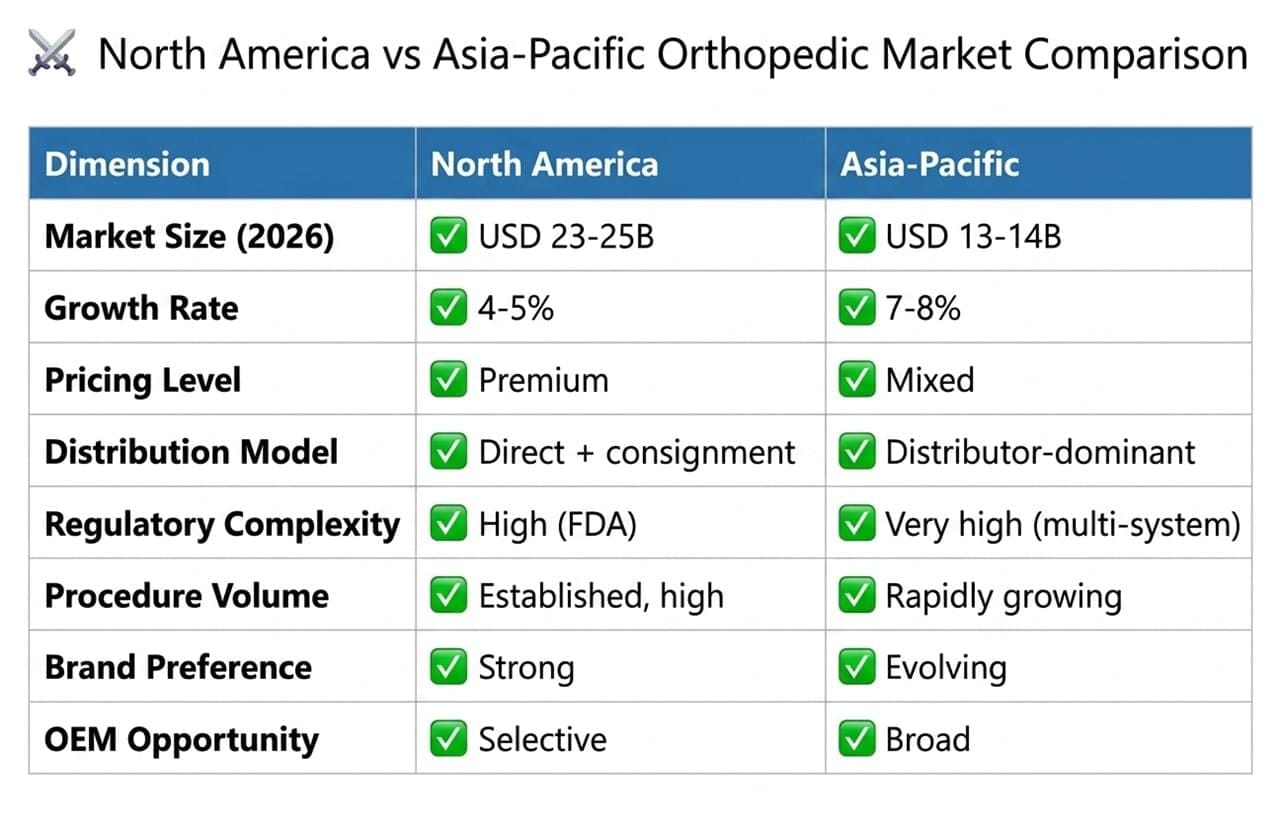 💸整形外科市場における価格差と戦略的影響
💸整形外科市場における価格差と戦略的影響
重要な洞察 北米とアジアの整形外科市場の比較 価格差が大きいのは、以下の点です。
- 🇺🇸 アメリカ合衆国: チタン製インターロッキングネイル = 350~450米ドル
- 🇨🇳 中国 (VBP): 40~80米ドル
- 🇮🇳 インド: 80~120米ドル
🔍 戦略的意味合い:
- ⚙️ コスト構造の乖離
アジア太平洋市場では、北米のコストモデルと比較して、リーン生産方式と低い間接費構造が求められる。. - 🧩 製品設計の適応
新興市場では、よりシンプルで耐久性のあるインプラントシステムが、複雑で高価なソリューションよりも優れた性能を発揮することが多い。. - 📊 規制投資のROI
FDAの承認費用はプレミアム価格設定によって正当化される一方、アジアでは市場固有の投資対効果(ROI)計算が必要となる。.
これらを理解する 整形外科用医療機器の規制の違い:FDAとアジア諸国 持続的な収益性を確保する上で鍵となる。.
🏗️ アジアの整形外科市場におけるOEMビジネスチャンス
の アジアの整形外科市場 より広範で柔軟なOEM/ODMの機会を提供します。
- 🇨🇳 中国
デュアルチャネル戦略:VBP(価値に基づく支払い)主導の公立病院とプレミアム私立病院 - 🇮🇳 インド
国内市場および輸出市場向けにコスト効率の高い製造パートナーシップに対する強い需要 - 🌍 地域輸出拠点
FDA/CE認証を取得したアジア拠点の製造業者は、国際的なブランドのグローバルサプライヤーとしての役割をますます担うようになっている。
❓ よくある質問:北米とアジアの整形外科市場の比較
Q1:どちらの市場規模が大きいですか?
総規模では北米がトップだが、アジア太平洋地域はより速い成長を示している。.
Q2:どちらの地域の方が規制が複雑ですか?
FDAは中央集権的で厳格だが、アジアでは複数の規制制度が存在し、全体的な複雑さが増している。.
Q3:FDAの承認はアジア市場への参入を後押しできますか?
はい、しかしそれは現地の承認手続きに取って代わるものではありません。特定の国では審査プロセスを迅速化できる可能性があります。.
Q4:中国のVBP政策はどのような影響を与えていますか?
これにより、公立病院におけるインプラントの価格が大幅に引き下げられ、競争力学が大きく変化した。.
Q5:アジア太平洋地域への最適な参入戦略は何ですか?
まずはFDA/CE認証を取得し、販売代理店を通じて事業を拡大し、中国を独立した戦略市場として扱う。.
✅結論
の 北米整形外科市場 北米とアジアの整形外科市場は、根本的に異なる機会特性を持っています。北米は高価格帯で手術件数も多いものの、高度な規制対応と資本集約型の流通網が求められます。一方、アジア太平洋地域は世界で最も高い成長率を誇りますが、複数のシステムにわたる規制遵守、価格最適化された製品設計、そして販売代理店に依存した市場参入が必要となります。.
最も成功している整形外科機器メーカーは、北米向けには高級製品ライン、アジア太平洋地域向けにはコスト最適化された認証製品といったように、それぞれの地域に合わせた戦略で事業を展開しています。戦略の詳細については、メインガイドをご覧ください。 世界の整形外科用医療機器市場.
北米またはアジア太平洋地域の整形外科市場への参入をご検討中ですか? 当チームにお問い合わせください 規制戦略および流通パートナーシップに関するガイダンスについて。.